- ホーム
- >
- 細胞生物学用語集トップ
- >
- 新着細胞生物学用語集(%E8%86%9C%E9%AA%A8%E6%A0%BC%E3%83%BB%E7%B4%B0%E8%83%9E%E8%86%9C%E5%BD%A2%E7%8A%B6%E5%88%B6%E5%BE%A1)
新着細胞生物学用語集(%E8%86%9C%E9%AA%A8%E6%A0%BC%E3%83%BB%E7%B4%B0%E8%83%9E%E8%86%9C%E5%BD%A2%E7%8A%B6%E5%88%B6%E5%BE%A1)
| ERMファミリー |
|---|
| 【ERM family】 |
| 田村 淳・月田 早智子 |
| 大阪大学大学院生命機能研究科 |
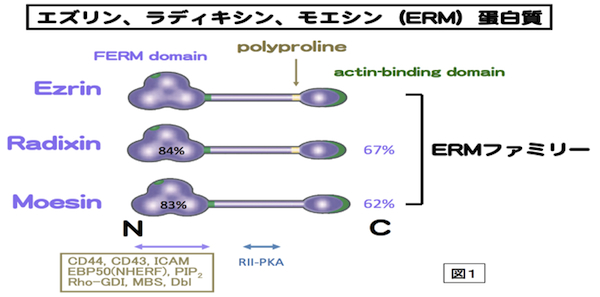
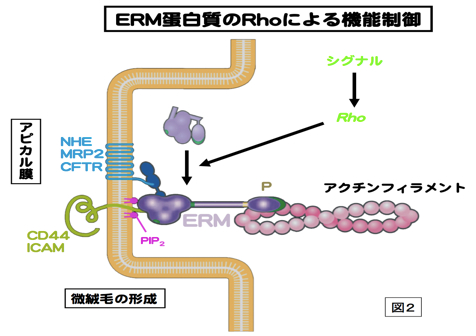
細胞骨格の1つであるアクチンフィラメントと細胞膜との動的な相互作用をつかさどる蛋白質ファミリー。微絨毛や神経成長錐、細胞分裂時の収縮環などアクチンフィラメントが細胞膜に結合する部分に局在する。アミノ酸レベルで75%程度の相同性を持つ3つの蛋白質Ezrin,Moesin,RadixinによりERMファミリーが形成され、各々の構成蛋白質はERM蛋白質とよばれる。いずれもN末側からFERMドメイン、α-ヘリックス領域、アクチン結合モチーフの順に並ぶドメインを持つ、分子量75kDaほどの分子である(図1)。エズリンとラディキシンは、モエシンにはないポリプロリンモチーフを余分に持つ。ERM蛋白質は、細胞膜-アクチンフィラメントを架橋する棒状の活性型と球状の不活性型の2つのコンフォメーションをとる。ERM蛋白質はRhoの下流で、PIP2により活性化されて、細胞膜とアクチンフィラメントに、各々、N末のFERMドメインとC末で結合すると考えられる。活性化型ERM蛋白質はC末のトレオニン残基のリン酸化により、安定化される。細胞膜との結合では、CD44などの細胞膜蛋白質に直接結合する場合と、トランスポーターなどの細胞膜蛋白質にPDZドメインをもつEBP-50を介して結合する場合がある(図2)。各々のERM蛋白質は、培養細胞では共発現することが多く、同じ局在を示すことも多いが、生体組織レベルでは、組織の種類によって異なる発現と局在を示す。例えば、肝細胞ではRadixinの発現が多く、腸管上皮細胞ではEzrinが、血管内皮細胞ではMoesinが多く発現している。Radixin、Ezrinのノックアウトマウスでは各々肝臓および胃の上皮細胞において、MRP2やHK-ATPaseのアピカル細胞膜への局在不全のためにDubin-Johnson型の高ビリルビン血症や胃酸分泌障害になる。上皮細胞アピカル表層構築に重要な蛋白質として、注目されている。参考文献 Tsukita, S., Yonemura, S. (1999)
Kikuchi, S., Hata, M., Fukumoto, K., Yamane, Y., Matsui, T., Tamura, A., Yonemura, S., Yamagishi, H., Keppler, D., Tsukita, S., Tsukita, S. (2002) Fehon, RG., McClatchey, AI., Bretscher, A. (2010) Arpin, M., Chirivino, D., Naba, A., Zwaenepoel, I. (2011) Neisch, AL., Fehon, RG. (2011) |
| リポソームと細胞骨格(アクチン、微小管、セプチン) |
|---|
| 【Reconstruction of cytoskeletons (actin, microtubule or septin) using liposome】 |
| 滝口 金吾・滝口 陽子 |
| 名古屋大学大学院理学研究科 |
| お問合せ |
| 生体膜の形態形成や動態制御の機構をインビトロの系で研究する際、膜のモデルとして巨大人工脂質膜小胞(巨大リポソーム、giant liposome、giant vesicleまたはgiant unilamellar vesicleなど)がよく使われる。巨大リポソームは、脂質二重膜(lipid bilayer、脂質二分子膜など色々な呼び方がある)が水溶液中で自然に閉じてできる人工膜小胞(liposome またはvesicle)の中でも直径がμmオーダー以上のものをそのように呼ぶ [1, 2]。細胞と同程度の大きさであり、位相差、蛍光、微分干渉、暗視野などいろいろな光学顕微鏡法で直接観察ができる利点を持つ。 巨大リポソームの作製には、試験管内に作製したリン脂質を主成分とする脂質フィルムに水溶液を加え静置して得る静置水和法(gentle hydration、natural swellingなど)や [3-5]、白金や透明導電ガラス(ITO (indium tin oxide)ガラスが多く用いられる)の表面にリン脂質を主成分とする脂質を塗布しておき、水溶液中で交流電圧を印加して作るエレクトロフォーメーション法(electro formation)が主流である [6]。最近は、界面通過法(spontaneous transfer)など、油水界面にできる脂質の単層の膜(lipid monolayer、これも脂質一分子膜など色々な呼び方がある。単層の脂質二重膜との混同に注意!)を利用して作製する新たなリポソーム作製法も開発され、より広汎な条件下、より良い効率で巨大リポソームが得られるようになってきている [7, 8]。 細胞骨格と生体膜との相互作用を見る目的で、アクチンや微小管、セプチンなどを巨大リポソームに再構成させる場合には2通りある。 1つは、巨大リポソーム内に細胞骨格蛋白質を封入し、リポソーム内部の空間で再構成させる方法である。静置水和法やエレクトロフォーメーション法でリポソームを作製する際に、重合前のG-アクチンやチューブリンを含んだ水溶液を使うと、自然に内部にG-アクチンやチューブリンを取り込んだ巨大リポソームが形成されてくる。このリポソームの形成後に温度の上昇や塩の内部供給によって、リポソームの内部でアクチン線維や微小管の重合を起こさせることができる [3, 4, 9]。また界面通過法などの手法を用いれば、既に重合してできたアクチン線維やアクチンの束もリポソーム内部に再構成することが可能である [7, 8]。 もう1つは、予め作製しておいた巨大リポソームを含む溶液に、灌流装置を用いて細胞骨格蛋白質溶液を添加することにより、リポソームの外部から相互作用させ、その表面で再構成させる方法である。セプチンの膜結合能の検証および膜突起誘導活性の発見は、この方法によって成された [5]。 リポソームの作製は容易で観察法も様々あるので、膜の研究を行う際に大変有効である。しかし、巨大リポソームに限らず、リポソームを用いて実験しようとするときには以下のことに留意する必要がある。リポソームの作製にどのような手法を用いるにしても、脂質組成や作製時の温度、溶液条件が、作製効率ならびに作製されてくるリポソームのサイズや形態に大きく影響する。特に作製時に使う水溶液が2価の陽イオンや高濃度の塩を含む場合、多層の脂質二重膜からできた膜小胞(multilamellar vesicle)や、脂質二重膜を形成仕損なった脂質分子が凝集してできた油滴(lipid droplet)などが形成されてくるので、リポソームとの混同に注意しなければならない。生理的な塩濃度など高い塩濃度条件下でリポソームを使用したり作製したりするためには、先ず等張の糖を含む溶液で作製しておいたリポソームを実験に使う、脂質組成にPEG(polyethylene glycol)を結合させた脂質を加えて作製する、界面通過法などのような手法を用いてリポソームを作製する、などの工夫が必要である [5-9]。 参考文献[1] R. Lipowsky, Nature 349, 475-481 (1991)
[2] H. Hotani et al., Biosystems 71, 93-100 (2003) [3] M. Honda et al., J. Mol. Boil. 287, 293-300 (1999) [4] T. Kaneko et al., J. Mol. Boil. 284, 1671-1681 (1998) [5] Y. Tanaka-Takiguchi et al., Curr. Biol. 19, 140-145 (2009) [6] T. Wollert & J.H. Hurley, Nature 464, 864-869 (2010) [7] K. Takiguchi et al., Langmuir 27, 11528-11535 (2011) [8] K. Takiguchi et al., Methods Enzymol. 464, 31-53 (2009) [9] L. Limozin et al., Phys. Rev. Lett. 95, 178101 (2005) |
| BAR ドメイン |
|---|
| 【BAR domain】 |
| 千住 洋介・末次 志郎 |
| 東京大学 分子細胞生物学研究所 細胞形態研究分野 |
| お問合せ |
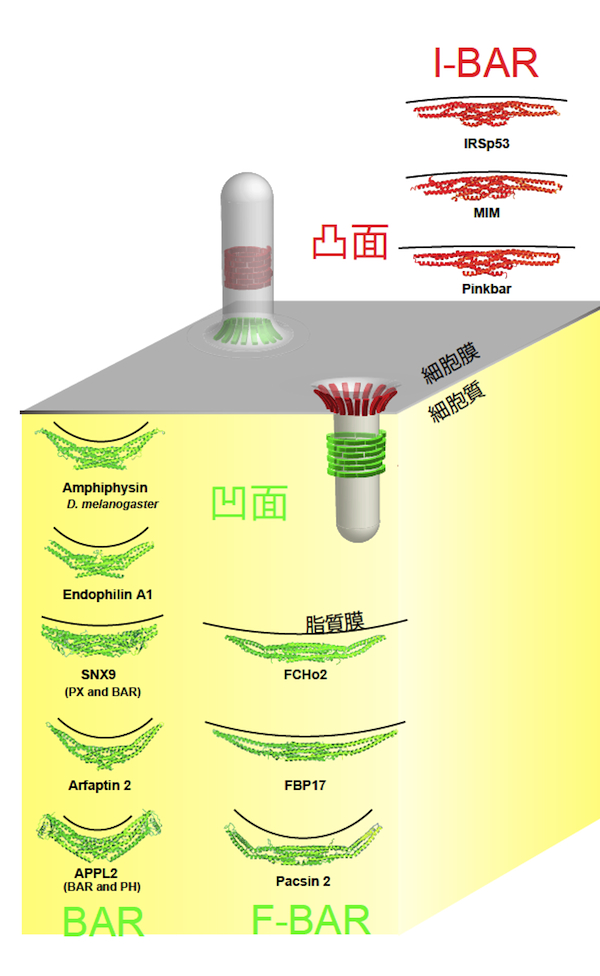
BAR (Bin/Amphiphysin/Rvs) ドメインスーパーファミリーは、BARドメインと総称される、BARドメイン、F-BARドメイン、I-BARドメインのサブファミリーに分類されるドメインを持つ。BARドメインおよびF-BARドメインは、三日月形の二量体を形成し、負に帯電している細胞膜と静電的な相互作用で結合する【画像1】。BARドメインとF-BARドメインは、三日月型二量体の立体構造における凹面が正に帯電している。この結合様式は、細胞膜の陥入構造に対応すると考えられ、実際に、多くのBARドメイン含有タンパク質 (Amphiphysin やEndophilinなど) や、F-BARドメイン含有タンパク質 (FBP17やFCHo1など) は、エンドサイトーシスなどの細胞膜の陥入構造の形成に関与する。一方、IRSp53等に含まれるI-BARドメインは、凸面が正に帯電している。よって、陥入構造とは逆の形態である、フィロポディアなどの細胞膜の突起構造の形成に関与する。また、BARドメイン、F-BARドメイン、I-BARドメインの中には、両親媒性ヘリックスなどの脂質膜に挿入されると考えられる部位を持つものがあり、この部位の挿入は、細胞膜の曲率形成を促進する。全体として、BARドメインスーパーファミリーは、細胞膜の曲率を認識、あるいは生成する機能を有すると考えられている。多くのBARドメイン含有タンパク質は、SH3ドメイン等の他のドメインを伴う。このため、BARドメイン含有タンパク質は、膜の曲率に準拠して、タンパク質を集積させる可能性がある。代表的なSH3ドメイン結合タンパク質は、Arp2/3複合体を活性化するWASPファミリータンパク質や、細胞膜を切断するダイナミン (dynamin) である。参考文献 |
| セプチン |
|---|
| 【Septin】 |
| 上谷 大介・木下 専 |
| 名古屋大学大学院理学研究科 生命理学専攻 情報機構学講座 |
| お問合せ |
セプチンは細胞質分裂(septation)・細胞極性・細胞形態の異常を呈する出芽酵母変異体の責任蛋白質として同定された重合性GTP結合蛋白質とそのホモログの総称である。セプチンファミリーはRas様のGTP/GDP結合領域をコアドメインとして共有し、多くはカルボキシル側にコイルドコイル配列を持つ。セプチン遺伝子は菌類からヒトまでの真核生物で進化的に保存され、出芽酵母では7種類、線虫では2種類、ショウジョウバエでは5種類、マウスでは13種類、ヒトでは14種類存在するが植物には存在しない。セプチンは多様な組み合わせでフィラメント状ヘテロオリゴマーを形成し、さらに環状線維束を形成したり人工リン脂質膜上で2次元格子を形成するなど独特の高次集合性を持つ。セプチンを主成分とする環状構造体としては出芽酵母の分裂溝直下に形成されるセプチン・リング(septin ring)がよく研究されてきた。セプチン・リングは細胞周期進行および細胞質分裂関連分子を集積させる足場(scaffold)としての役割と、細胞膜および内膜系上を流動する膜蛋白質の非対称性分布を保つ拡散障壁(diffusion barrier)として母-娘細胞を区画化する役割を持つことが報告されている。細胞質分裂の分子機構は種間・系譜間の多様性が著しく、セプチン・リングが明確に同定できない場合も多いが、セプチンの要求性は種を超えて保存されている。多細胞生物におけるセプチンの発現はむしろ分裂後の細胞に多いため、細胞質分裂以外の機能に興味が持たれている。哺乳類においては、精子鞭毛内(輪状小体)と繊毛基部の細胞膜直下にセプチンを主成分とすると推測される環状構造体が存在し、足場・拡散障壁機能以外に細胞表層剛性維持機能を持つことが示されている。哺乳類のセプチンの一部は非筋型ミオシンと相互作用することにより、アクトミオシンを主成分とする収縮輪やアクチンストレス線維(actin stress fiber)の維持に寄与するが、詳細は不明である。ヒトでは優性変異型SEPT9 が家族性神経痛性筋萎縮症の原因となるほか、パーキンソン病、統合失調症、精子無力症では複数のセプチンの量的・質的異常が随伴する。参考文献木下 専 蛋白質 核酸 酵素 54, 1150-1158 (2009)
Weirich CS, Erzberger JP, Barral Y. The septin family of GTPases: architecture and dynamics.Nat Rev Mol Cell Biol. 9(6):478-89, 2008. |

 HOME
HOME